Page 9 - Vol.07
P. 9
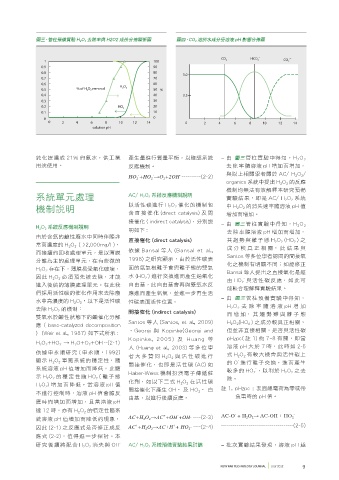
圖三、管柱預備實驗 H 2 O 2 去除率與 H2O2 成份分佈關係圖 圖四、CO 2 溶於水成分受溶液 pH 影響分佈圖
2
1 100 CO 2 HCO 3 CO 3
0.9 90
0.8 80 1.0
0.7 70
0.6 H 2 O 2 60
0.5 % of H 2 O 2 removal 50 %
0.4 40 0.5
0.3 30
0.2 HO 2 – 20
0.1 10
0 0
0 2 4 6 8 10 12 14 0 2 4 6 8 10 12 14
solution pH pH
純化提濃成 21% 的氨水,供工業 產生量進行質量平衡,以確認系統 – 由 圖三管柱實驗中得知,H 2 O 2
用途使用。 反應機制。 去 除 率 隨溶液 pH 增加而增加,
-
-
-
HO 2 +HO 2 →O 2 +2OH ----------(2-2) 與以上相關學者關於 AC/ H 2 O 2 /
organics 系統中提出 H 2 O 2 的反應
機制均無法有效解釋本研究預備
系統單元處理 AC/ H 2 O 2 系統反應機制說明 實驗結果,即是 AC/ H 2 O 2 系統
以活性碳進行 H 2 O 2 催化的機制包 中H 2 O 2 的消失速率隨溶液 pH 值
機制說明
含 直 接 催 化 (direct catalysis) 及 間 增加而增加。
接催化 ( indirect catalysis),分別說
H 2 O 2 系統反應機制說明 – 由 圖三 管柱實驗中得知,H 2 O 2
明如下 : 去除率隨溶液 pH 增加而增加,
由於含氨的鹼性廢水中同時伴隨非 -
直接催化 (direct catalysis) 其趨勢與離子態 H 2 O 2 (HO 2 )之
常高濃度的 H 2 O 2 ( >2,000mg/l ), 成分較具正相關,此結果與
依據 Bansal 等人 (Bansal et al.,
而接續的回收處理單元,是以薄膜 Santos 等多位學者認同的間接氧
分離為主的處理單元,在有些微的 1998) 之研究顯示,由於活性碳表
化之機制有明顯不同;如能修正
H 2 O 2 存在下,薄膜易受氧化破壞, 面的氫氧根離子會與離子態的雙氧 Bansal 等人提出之直接氧化是經
-
因此 H 2 O 2 必須預先被去除,才能 水 (HO 2 ) 進行交換進而產生過氧化 -
由 HO 2 與活性碳反應,如此可
進入後續的薄膜處理單元。在此我 自由基,此自由基會再與雙氧水反
能較合理解釋實驗結果。
們採用活性碳的催化作用來去除廢 應進而產生氧氣,並進一步再生活
– 由 圖三 管柱預備實驗中得知,
水中高濃度的 H 2 O 2 ,以下是活性碳 性碳表面活性位置。
H 2 O 2 去 除率隨溶液 pH 增加
去除 H 2 O 2 的機制:
間接催化 (indirect catalysis) 而增加,其趨勢雖與離子態
雙氧水於鹼性狀態下的鹼催化分解
-
Santos 等人 (Santos, et al., 2009) H 2 O 2 (HO 2 ) 之成分較具正相關,
應 ( base-catalyzed decomposition
、Georgi 與 Kopinke(Georgi and 但並非直接相關,是否與活性碳
) (Weir et al., 1987) 如下式所示 :
Kopinke, 2005) 及 Huang 等 pHzpc( 註 1) 約 7~8 有關,即當
-
-
H 2 O 2 +HO 2 →H 2 O+O 2 +OH --(2-1)
人 (Huang et al., 2003) 等 多 位 學 溶液 pH 大於 7 時,此時如 2-5
依據申永順研究 ( 申永順,1992)
者大多贊同 H 2 O 2 與活性碳進行 式H 2 O 2 有較大機會與活性碳上
顯示 H 2 O 2 單獨系統的穩定性,隨 的O 進行離子交換,進而產生
-
間接催化,也即是活性碳 (AC) 如
系統溶液 pH 值增加而降低,此顯 較多的 HO 2 ,以利於 H 2 O 2 之去
-
Haber-Weiss 機制扮演電子傳遞催
-
示H 2 O 2 的 穩 定 性 隨 HO 2 ( 離 子態 除。
化劑,如以下二式 H 2 O 2 在活性碳
H 2 O 2 ) 增加而降低。當溶液 pH 值
間接催化下產生 OH‧ 及 HO 2 ‧ 自 註 1. pHzpc : 表面總電荷為零或帶
不進行控制時,溶液 pH 值會隨反
由基,以進行後續反應。 負電時的 pH 值。
應時間增加而增加,且當溶液 pH
達12 時,亦有H 2 O 2 的穩定性隨系 - -
-
+
統溶液 pH 值增加而降低的現象, AC+H 2 O 2 →AC +OH +OH· ----(2-3) AC-O + H 2 O 2 → AC-OH + HO 2
+
+
因此 (2-1) 之反應式是否修正成反 AC +H 2 O 2 →AC+H + HO 2 · ----(2-4) -------------------------------------(2-5)
應式 (2-2),值得進一步探討。本
研究後續將配合 H 2 O 2 消失與 OH - AC/ H 2 O 2 系統預備實驗結果討論 – 批次實驗結果發現,溶液 pH 越
NEW FAB TECHNOLOGY JOURNAL JULY 2012 9