摘要
製程廢水中短鏈全氟化合物去除策略與設計規劃
Keywords / Perfluoroalkyl Substance(PFAS),Perfluoro Butane Sulfonic Acid(PFBS),Activated Carbon2,Wastewater Treatment
半導體界近年積極開發工業再生水技術,將自身排放的工業廢水再製供前段製程重新使用,廢水中不易被水處理系統去除的短碳鏈全氟化合物,雖然台灣目前未有制訂法規管制排放濃度,但已開始被重視是否影響再生水水質。本研究探討多方文獻,評選半導體廠最適處理方法,並針對該法分析材質差異對於去除成效的影響,最後導入技術於實際工廠運轉測試。
活性碳顯示於酸性時擁有最高的全氟化合物去除率,分析三種不同廠牌活性碳特性,在實驗室各項測試發現原料為煙煤的活性碳去除效果大於椰殼碳。將顆粒煙煤碳於工廠端建置連續廢水進流過濾塔,並同步分析多股製程廢水,將含有此類物質之廢水配置專管集中納入處理,結果顯示系統端去除率可長期穩定達99.9%以上,多廠再現性驗證放流總去除率亦皆達93.3%以上,證實本方法為確實有效且可實際快速導入應用之途徑。
The semiconductor industry has been developing industrial reclaimed water technology, which recycles the industrial wastewater discharged by itself for reuse in the manufacturing process. The short-chain Perfluoroalkyl Substance(PFAS) in the wastewater are not easily removed by the water treatment system, the study surveys the most suitable removal method for factories, discusses the material differences on the removal rate, then finally introduced into the factory operation.
Granular Activated carbon(GAC) shows the highest PFAS removal rate under acid condition in the study. Characteristics of three different brands of activated carbon are analyzed in laboratory tests. It is found that the removal rate of bituminous coal is greater than coconut coal. Filters filled with bituminous coal are installed in the factories and served with continuous wastewater inflow. With wastewater drains containing with PFAS are identified and piped into the system, the results show that the removal rate at the system end can be more than 99.9% constantly. According to the multi-plant reproducibility verification, the final effluent improvement rates are all more than 93.3%. It is proved that the method is indeed effective and can be practically introduced into the fab operation.
1. 前言
2021年是台灣近50年來水情最為嚴峻的一年,水對於晶圓製造是不可或缺的,水資源的發展刻不容緩。且近幾年環保意識高漲,發展可替代自來水的新興水源,不但可以增加水源穩定降低旱災帶來的傷害,還可促進水資源再利用以接近水資源正效益的目標。做為先驅者,台灣半導體晶圓製造業者為因應未來氣候變遷與實踐綠色製造,工廠端不僅持續強化用水效率,並開始嘗試將再生水導入半導體製程使用,希望藉由再生水的技術開發,長期可成為一項穩定供應的水源,並緩解台灣水資源因季節分配不均的問題,降低自來水需求負擔,達到穩定運轉與永續發展的目標。
再生水主要來源為民生污水與工業廢水的回收再利用,然而民生污水水質比較難以穩定控制。為了能夠成功取代自來水,且不影響晶圓廠運轉及製造品質,前期需進行一系列的水質檢測及驗證規劃,方可達成逐步的安全取代。過往經驗顯示,晶圓廠內使用的超純水處理系統對於小分子有機碳去除能力不佳,因此,針對此類物質會進行更深入的檢測分析,及導入前的去除模擬以因應可能發生的狀況。近年各界高度關注的全氟或多氟烷基化合物(Perfluoroalkyl Substance, PFAS),通稱為全氟化合物,尤其是長碳鏈的全氟辛酸(Perfluoro Octanoic Acid, PFOA)、全氟辛烷磺酸(Perfluoro octane sulfonic acid, PFOS)及其相關物質,證實對人體健康及環境造成危害。國際《斯德哥爾摩公約》將PFAS列為持久性有機污染物,歐盟也限用此化合物並定期進行監控。美國環保署除了持續監控及評估健康影響外,也訂定了飲用水中的健康公告數值(Health advisory levels)為70ng/L(ppt),並與工業界一同制訂PFOA與PFOS逐步減量計畫。隨半導體先進製程發展,目前晶圓廠禁用此類分子結構中碳原子數超過四個的全氟化合物,但還是有使用部分含四個碳及以下的短碳鏈全氟化合物,多半為全氟丁烷磺酸(Perfluoro butane sulfonic acid, PFBS),或者全氟丁酸(Heptafluorobutyric acid, PFBA)等羧酸類物質,研究顯示此類物質目前對人體或環境無顯著危害性,且均未發現造成人體危害及環境污染的直接證據,但大量相關研究調查仍持續進行中。
雖然台灣目前對於此類短碳鏈全氟化合物之法規管制尚未明朗,但為了防範該物質隨著工廠排出的工業廢水,經過再生水處理流程無法完整去除,卻經由使用再生水後重新回流至製程端交叉污染,本研究需防範未然,尋找合適去除方法,將此新興污染物於廢水系統端之排放濃度盡可能降低至零,不僅能優化放流水體與河川水質,避免進入人體與食物鏈中,亦能確保未來半導體製程中使用的再生水品質無虞,達成環境與產品品質共榮共好的雙贏局面。
2. 文獻探討
2.1 全氟化合物化學特性及應用
PFAS為人工合成之化學物質,其化學結構中碳骨架上的氫原子會以部分或全部被氟原子取代,並於化學結構的末端帶有官能基團,另具有親水性/疏水性和高穩定的碳氟鍵(鍵能=110kJ/mol),故有高物化穩定性特點,因此許多工業製程與日常消費產品中皆有廣泛使用,例如消防泡沫、鹼性清潔劑、油漆、不粘炊具、地毯製品、室內裝潢、洗髮精、地板蠟、攝影膠片、農藥製劑、食品包裝、膠帶、假牙清潔劑及半導體製程等。
廢水處理廠為排放至環境水體的主要來源[1],現今已可於飲用水[2]、地下水[3]、河川[4][5]、海水[4]等環境水體中檢測到PFAS,成為了人類潛在暴露於PFAS的主要途徑。PFAS的物化穩定性高,不易被生物分解,故人體幾乎無法完全代謝,造成長時間累積於人體或生物體中[6]。根據研究指出,於挪威居民175個的血清樣本中可檢測到的PFOS,其統計之中位數的濃度最高達到25ng/mL,其次是PFOA,濃度可達到3.6ng/mL,且攝取海鮮為PFOS的主要來源[7]。另外,其處於人體的半衰期長,PFOS和PFOA平均半衰期分別為4.8年與3.5年,因此將對人體引起各種長期健康危害[8]。
針對台灣北部區域招募231名哮喘和225名非哮喘兒童,探討PFAS暴露與兒童哮喘之關聯性,其結果證實台灣兒童中PFAS的暴露與哮喘成正相關性[9]。另針對美國12至15歲的兒童,探討PFAS暴露與兒童注意力缺陷/多動障礙(Attention Deficit Hyperactivity Disorder, ADHD)之關聯性,證實ADHD的較高患病率與PFAS暴露具正相關[10]。美國環境保護署表明,越來越多的健康數據說明長期暴露於PFAS會造成健康危害,例如嬰兒出生體重低、免疫系統受損、甲狀腺激素破壞、癌症等。
2.2 全氟化合物之環境流佈與宿命
由於各國開始限制長碳鏈全氟化合物的使用,導致全球製程所用原料逐漸從長碳鏈轉變為短碳鏈全氟化合物,且早期環境中釋放的長碳鏈全氟化合物透過環境降解,也會轉化成短碳鏈全氟化合物,故短碳鏈全氟化合物的影響日益嚴重[11]。表1可知此類PFAS家族酸度係數(pKa)大多趨近於0或<0,顯示化學表現為強酸或中強酸,另短碳鏈家族由於水分配係數(log Kow)較長碳鏈低,水溶解係數(log Sw)較高,顯示其親水性與溶解性更好及流動性強,自然環境下的地下水和土壤吸附能力較差,因此於環境持久性更高,容易造成廣泛的環境影響[12][13]。現今已於極地地區的飲用水、沉積物、污泥,甚至雪和冰中廣泛發現了兩種最常見的短碳鏈全氟化合物,即PFBS和PFBA[14]。於中國黃河中下游處設立採樣點進行水質採樣,證實短碳鏈全氟化合物在水生環境中佔整個PFAS總量的88.8%,而長碳鏈的全氟化合物則大多出現在沉積物和懸浮顆粒上[15]。然而,現今短碳鏈的全氟化合物,如PFBS和PFBA的研究尚未完整,且對該物質未有完善的環境健康風險評估分析,因此目前還未有規範短碳鏈全氟化合物的使用與排放限值。
| PFASs | Chemical formula | Carbon number | Molecular weight(g/mol) | Log Sw(mol/L) | Log Kow | pKa |
| Long C-F Chain(C>4, forbidden) | ||||||
|---|---|---|---|---|---|---|
| Perfluorooctane sulfonic acid(PFOS) | CF3(CF2)7SO3H | 8 | 500.1 | -6.68 | 4.49 | -3.27 |
| Perfluorohenptane sulfonic acid(PFHpS) | CF3(CF2)6SO3H | 7 | 450.1 | -5.63 | 3.82 | <0.3 |
| Perfluorohexane sulfonic acid(PFHxS) | CF3(CF2)5SO3H | 6 | 400.1 | -4.27 | 3.16 | 0.14 |
| Perfluoropentane sulfonic acid(PFPeS) | CF3(CF2)4SO3H | 5 | 350.1 | -2.90 | 2.49 | <0.3 |
| Perfluorooctanoic acid(PFOA) | CF3(CF2)6COOH | 8 | 414.1 | -1.93 | 5.30 | -0.2 |
| Perfluorohenptanoic acid(PFHpA) | CF3(CF2)5COOH | 7 | 364.1 | -1.94 | 4.67 | -0.19 |
| Perfluorohexanoic acid(PFHxA) | CF3(CF2)4COOH | 6 | 314.1 | -1.16 | 4.06 | -0.16 |
| Perfluoropentanoic acid(PFPeA) | CF3(CF2)3COOH | 5 | 264.1 | -0.37 | 3.43 | 0.17 |
| Short C-F Chain(C≦4) | ||||||
|---|---|---|---|---|---|---|
| Perfluorobutane sulfonic acid(PFBS) | CF3(CF2)3SO3H | 4 | 300.1 | -1.53 | 1.82 | 0.14 |
| Perfluorobutanoic acid(PFBA) | CF3(CF2)2COOH | 4 | 214.1 | 0.42 | 2.82 | 0.4 |
| Perfluoropropionic acid(PFPrA) | CF3CF2COOH | 3 | 164 | 0.54 | 1.47 | -0.39 |
| Trifluoroacetic acid(TFA) | CF3COOH | 2 | 114 | 0.94 | 0.50 | 0.16 |
2.3 全氟化合物處理方法
2.3.1 高級還原法
高级還原為一種化學降解方法,主要透過產生高還原性自由基,如水合電子(e-aq)、氫原子(H•),來降解水中難分解污染物。去除率不管是使用高級氧化程序(Advanced Oxidation Processes, AOP)或高級還原程序(Advanced Reduction Processes, ARP)會取決於目標污染物的物化特性,許多難分解之新興污染物,以ARP降解的效果會比AOP更有成效[16][17]。
紫外光搭配亞硫酸鹽為ARP法其中之一,其分解全氟化合物的效率,不但取決於目標污染物的鍵結強度,還會受到水體中的pH值、溫度、溶氧、無機化物、亞硫酸鹽添加濃度、目標污染物的初始濃度、紫外光種類與強度等影響[18]。於本法降解PFOS、PFOA的研究中,證實長碳鏈全氟化合物會因化學鍵能結構而產生斷鍵反應,於中間產物分析結果發現短碳鏈全氟化合物,且其濃度於反應初期有提升而後再下降之趨勢,氟離子濃度隨反應時間有所提高[19] [20]。
2.3.2 濾膜法
現今薄膜技術應用於水處理日益廣泛,濾膜法對PFAS的去除率會受到其物化特性,如分子量、分子形狀、官能團、疏水性、電荷強度、pKa影響,此外也同時被濾膜的物化特性影響,包含濾膜的帶電性、疏水性、操作壓力以及水體水質參數等因素[21]。以逆滲透(Reverse Osmosis, RO)去除PFOS,其可有效阻絕濃度範圍為0.5-1500mg/L的PFOS,去除率可達到99%以上[22]。奈濾膜(Nanofiltration, NF)進行不同全氟羧酸化合物的去除研究指出,於溫度18℃、水體pH值為6.7的環境下,分別進料濃度均為1g/L的不同全氟羧酸化合物,經奈濾膜維持進流量在1L/min過濾,其去除率均可達到93%以上,然而仍可於滲透溶液中偵測到短碳鏈全氟化合物PFBS和PFHxS,濃度高達40ng/L,而長碳鏈全氟化合物與短碳鏈相比,長碳鏈較好被奈濾膜阻絕[23]。薄膜處理技術對PFAS的去除率佳,但投資成本高且耗能高,濾膜長期使用會有結垢生成、阻塞孔道,造成通量下降的問題。
2.3.3 直接光解與光催化氧化法
直接光解法主要利用低波長、高能量的紫外光降解水中的PFAS,無需再添加其他化學物質,然而由於其鍵結穩定難以破壞,故需要波長220nm以下或更高強度的紫外光才可進行脫氟降解。長碳鏈的PFAS可透過紫外光照射光解,產生連續脫烷基反應,但會導致短碳鏈副產物形成,如PFBS和PFBA,然而短碳鏈全氟化合物更耐光降解,故存在短碳鏈難以光解去除的問題[24]。PFOA的直接光解實驗,在紫外光照射120分鐘,PFOA的去除率為9%,脫氟率為5%,而於真空紫外光照射下,PFOA的去除率可提升達到87%,脫氟率達到25%,證實光強度會影響PFOA去除率與脫氟率[25]。
光催化氧化降解全氟化物,大多會使用半導體做光催化材料如二氧化鈦,利用低波長、高能量的紫外光照射光催化材料,產生電子-電洞對,水中氧分子與電子還原生成超氧自由基(O2-),而電洞會與H2O產生高反應活性的氫氧自由基(OH•),氫氧自由基具有氧化全氟化物的能力[26]。透過二氧化鈦與還原石墨烯氧化物(95%TiO2/5%rGO)的複合材料,證實以0.1g/L的複合材料於12小時可有效降解0.24mmol/L的PFOA,其去除率達到93±7%[27]。
2.3.4 電化學氧化法
電化學氧化降解PFAS的機制分為兩種,分別為陽極的直接氧化與間接氧化,由於PFAS去除效率取決於陽極材料的電子轉移能力、氫氧自由基生成能力和氧氣釋出電位,故現今研究大多以陽極的直接氧化的方式降解PFAS,影響因子包括電極特性、電流密度、電極距離、pH值、溫度、目標污染物初始濃度、電解液性質等[28]。使用摻硼金剛石作為陽極,以陽極直接氧化降解初始濃度分別為15mg/L與10mg/L的PFOA與PFOS,電流密度50mA/cm2,並配製濃度1500mg/L的Na2SO4和167mg/L的NaCl的電解質溶液,實驗證實PFOA、PFOS於8小時內均達到完全降解的成效[29]。針對短碳鏈的PFBS電化學氧化降解,利用摻硼金剛石作為陽極,於溫度22°C、電流密度10mA/cm2,降解初始濃度為0.4mM的PFBS,於反應60分鐘可達到90%的降解[30]。
2.3.5 超聲波氧化法
超聲波氧化法主要透過頻率範圍20到1000kHz的聲波傳送能量至水體,使水中氣泡發生空穴作用,產生高濃度、高反應活性的氫氧自由基,進一步氧化水中有機污染物,當空穴作用發生時,會造成瞬時氣泡破裂會促使內部平均蒸氣溫度提高到4,000K。在通入氬氣的水體中,以超聲波氧化分解PFOS及PFOA的研究中指出,控制水體溫度10℃、初始濃度為12μΜ與10μM,以頻率618kHz的超聲波進行降解,於三小時內PFOA與PFOS的脫氟率均達到90%以上,同時產生短碳鏈全氟化合物[31] ; 另利用同法相同條件降解PFBS,於120分鐘內去除率可達到50%[32]。本法由於需要消耗較多能量,單獨使用降解有機污染物較不符合經濟效益,故大多會搭配氧化劑以提高難降解污染物的降解效率。
2.3.6 活性碳吸附法
活性碳為廣泛使用的吸附材,具有低耗能、操作簡單、可大規模應用於實廠廢水處理等優點。其對PFAS的吸附效能,取決於吸附劑與PFAS之間的物理化學吸附作用,其包含靜電相互作用、疏水相互作用、H鍵、π-π鍵、凡得瓦力、離子交換作用等,故PFAS對不同的吸附劑有著顯著差異[33]。另外,去除率亦會受到PFAS的物化特性,如分子大小、官能基、親水性、解離常數(pKa),以及吸附劑的孔洞大小、形狀、比表面積、吸附容量、表面官能基,以及環境水體中的pH值、無機離子和天然有機物等多重特性所影響[21]。
活性碳具有高比表面積與吸附能力,且由於其表面為疏水性,故對疏水性有機物具有極好的吸附效能。早在2005年,美國3M公司已利用顆粒活性碳柱處理含有PFOA濃度2mg/L的廢水,且PFOA去除率可達到99%以上[34]。透過不同化學氧化及物理方法來去除水中PFOA與PFOS,以顆粒狀活性碳(Granular Activated Carbon, GAC)吸附為最佳的去除方法,PFOA與PFOS的平均去除率均達到90%[35]。針對活性碳吸附PFBS之研究,確認GAC對於PFBS存在吸附特性,當水相中PFBS達平衡濃度為27mg/L時,吸附到活性碳上的PFBS的濃度為48mg/g[36]。另由等溫吸附曲線探討,亦證實GAC可有效吸附PFBS,且活性碳會產生多層吸附,並出現孔洞凝結的現象[37]。
3. 研究方法與特性分析
3.1 處理方法與目標污染物選定
彙整上述眾多處理長、短碳鏈的全氟化合物方法,[38]歸納了數種處理PFOA和PFOS物質之技術去除率比較顯示於 圖1,此結果可以看到逆滲透濾膜法或活性碳吸附法等分離技術的去除率,平均表現皆較高級氧化技術,以及較其他介質吸收法優秀,其中又以GAC活性碳對於PFOS及PFOA的吸附實驗中皆獲得最高之去除率(>90%)。實際應用上,高級氧化/還原技術若能確保藥劑、光源穩定供應,其處理程序可以不中斷的進行,而分離技術需要考慮再生、清洗、定期更換,故需要數個反應器確保處理程序不中斷,彼此間方法選定仍需依靠實際工廠運轉特性做優劣勢取捨。
圖1、PFOS與PFOA處理技術去除率比較[38]
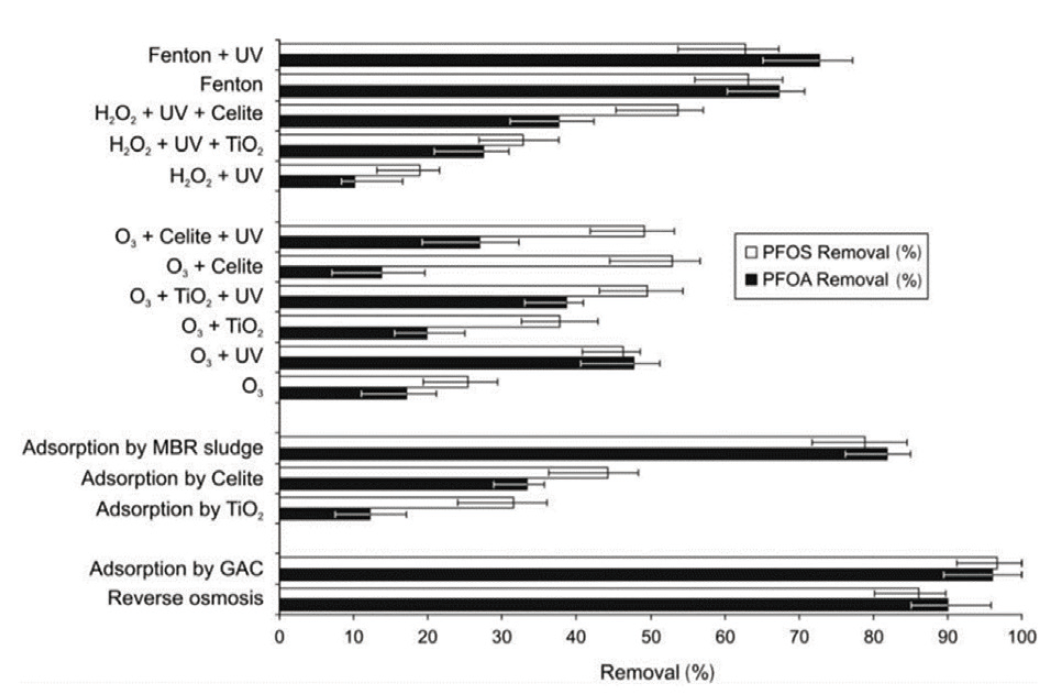
以晶圓廠而言,工廠內既有的廢水回收系統大量使用活性碳去除水中的雜質,以及分解半導體製程廢水中的氧化性物質,此方法已導入數十年,在實廠運轉中並不陌生,為成熟且穩定的可靠技術。對照前述PFAS的數種去除方法,若以提供能量斷鍵的分解方式,多半會衍生短碳鏈全氟化合物碎片殘留與增生,單獨對短碳鏈使用的去除效果亦更差 ; 濾膜法需考量膜面破損後滲透,及小分子有機碳易於穿透之可能性,相比而言,活性碳吸附法擁有最高之去除率,其物理吸附機制相對穩定,又以此法針對既有廠內系統增設與修改、成本考量乃至於後續的運轉維護,實為最簡易快速的途徑。
綜歸上述文獻資訊,以及考量廠內實際廢水特性與系統架構,本研究選定以短碳鏈的PFBS作為實驗目標污染物,利用GAC活性碳吸附法分離廢水中的PFBS,探討其最佳去除之操作條件。PFBS為四個碳所組成之全氟化合物,化學結構之親水端為磺酸基(Sulfonyl Hydroxide)組成,PFBS結構及物化特性如 表2所示,其pKa為0.14,顯示於環境水體中大多屬於解離狀態。
| 資訊 | 目標污染物 |
|---|---|
| 中文名稱 | 全氟丁烷磺酸 |
| 英文名稱 | Perfluorobutanesulfonic acid(PFBS) |
| CAS No. | 375-73-5 |
| 化學式 | C4HF9O3S |
| 結構式 | 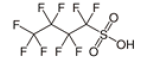 |
| 分子量(g/mol) | 300.10 |
| 密度(g/mL) | 1.811 at 25°C |
| 沸點 | 211°C |
| pKa | 0.14 |
| Log Sw(mol/L) | -1.53 |
| Log Kow | 1.82 |
3.2 活性碳材質差異分析
本實驗使用三種不同廠牌之GAC顆粒活性碳,進行特性分析與吸附試驗,分別為中國炭素工業股份有限公司G-840 (簡寫為A)、兆聯實業股份有限公司TAC-0830-ASX(簡寫為MU)及Calgon Carbon Co. F400(簡寫為F400)。首先,針對三種活性碳物化特性分析分為以下三部分,以了解不同廠牌之顆粒活性碳吸附特性後,再進行PFBS之吸附測試。
3.2.1 界達電位分析
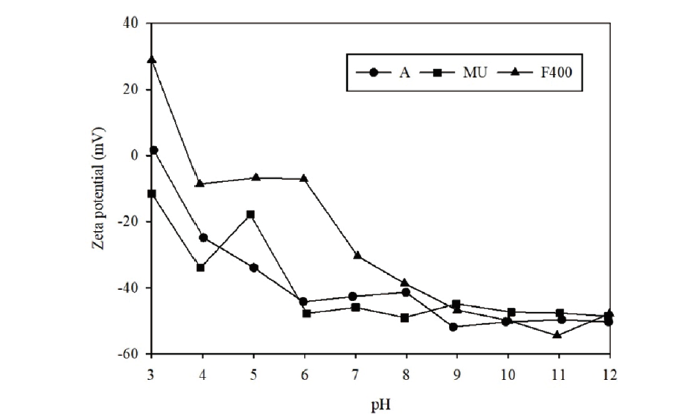
藉由量測界達電位分析,可以了解材料在不同pH質條件下的表面帶電特性。圖2為三種活性碳材質之界達電位分析結果,考量儀器材質強酸鹼之不耐受性,訂定測試pH範圍3~12。活性碳A的零電位點pH值(pHpzc)為3.11,當pH<3.11時,表面帶正電;當pH>3.11時表面帶負電。活性碳MU的實驗pHpzc值雖然無法由圖中得知,但在本實驗pH=3~12的條件中可知其表面皆帶負電。活性碳F400的pHpzc為3.73,當pH<3.73時,表面帶正電;當pH>3.73時表面帶負電。由此結果得知,若選用F400做為吸附介質時,將操作pH條件控制低於3.73時,預期將較易吸附水中幾乎為解離狀態,帶負電荷的PFBS。相對其他兩者活性碳,欲使其表面帶正電荷,操作環境pH需再往下才能達到相同條件,較不易達成。
圖2、界達電位分析
3.2.2 比表面積與孔徑分析
根據國際純化學和應用化學聯合會(International Union of Pure and Applied Chemistry chemical nomenclature, IUPAC),77K的氮氣等溫吸脫附曲線分為六種形式,遲滯曲線分為四種形式,如 圖3所示。三種GAC的氮氣等溫吸脫附曲線如 圖4所示,可以看出三者的吸脫附曲線皆接近於type IV曲線,並具有遲滯現象,為典型的中孔型材料。當壓力上升,氮氣會在孔壁上被多層吸附,若壓力持續上升,因吸附質增加導致氣相分子活動空間減少,此時分子間的凡德瓦力增強使氣相分子可在低於飽和蒸汽壓情況下凝結,造成高壓條件下吸附量快速上升,此即毛細冷凝現象(capillary condensation)。在脫附階段,因毛細冷凝現象造成吸附量多於其他種類吸附曲線,需要較低的壓力才能全部脫附,因此產生吸附與脫附路徑不同之遲滯現象。從 圖3中可看出活性碳A和MU的遲滯迴線接近水平且平行,屬於H4形式,其孔洞型態為狹縫型孔洞(narrow slit-like pore);活性碳F400在高壓區為向上攀升的曲線,並且遲滯迴線無水平且平行的特徵,屬於H3形式,其孔洞型態為平板狀(plate-like)粒子聚集排列形成狹縫型孔洞(slit-shaped pore)。
圖3、(a)氮氣等溫吸脫附曲線分類;(b)遲滯形式分類
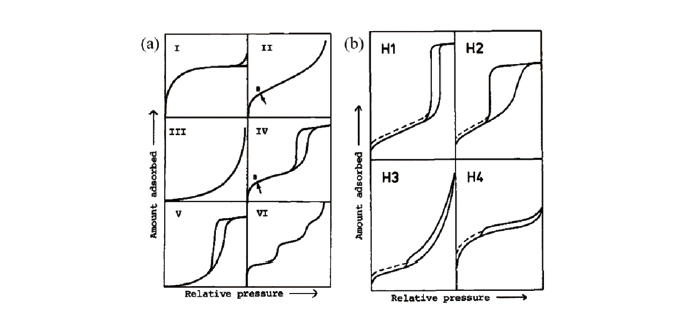
圖4、三種GAC之氮氣等溫吸脫附曲線
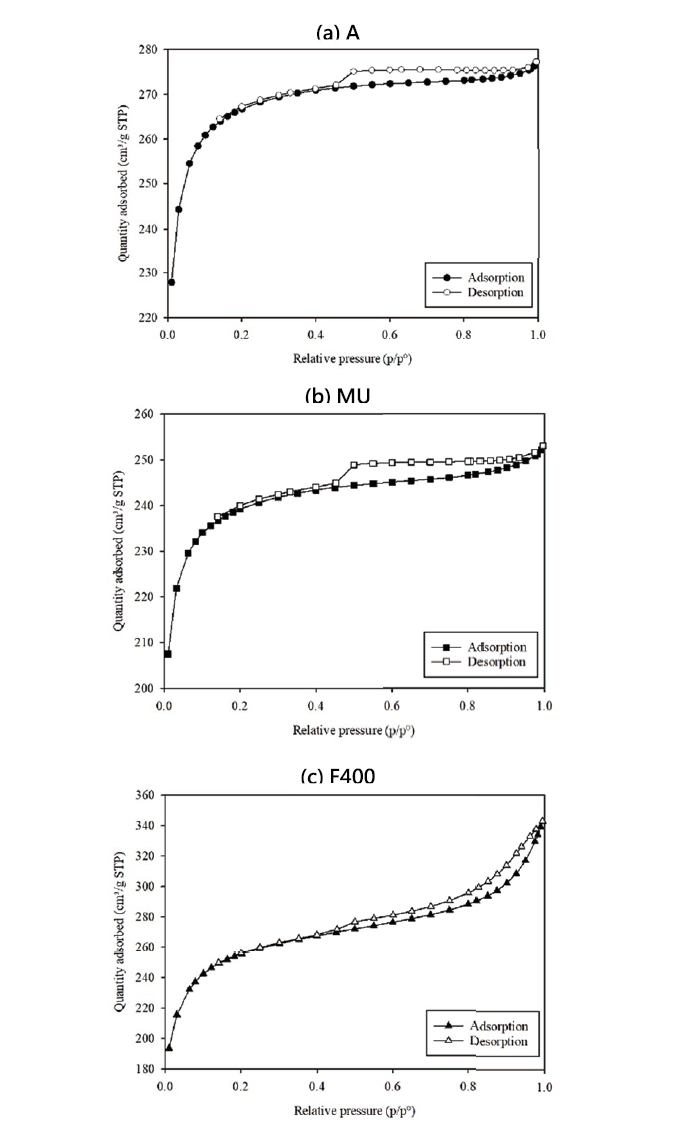
量測三種GAC的比表面積與孔徑分析結果如 表3所示,其中微孔面積、外部面積、微孔體積三者是以t-plot方法計算,BET比表面積是BET比表面積測試法(Brunauer, Emmett, Teller Method)的簡稱,代表1公克固體所佔有的總表面積,可由微孔表面積和外部面積相加計算出。一般商用活性碳的比表面積大約為1000m²/g,而結果顯示BET比表面積最高者為活性碳A(806.90m²/g)。以微孔的表面積和體積比例來看,活性碳F400的比例較其餘兩者低,顯示出具有較高比例的中孔表面積和體積,以平均孔徑來看,F400的孔徑確實大於其餘兩者。
| 活性碳類型 | A | MU | F400 |
|---|---|---|---|
| BET比表面積(m2/g) | 806.90 | 722.88 | 791.35 |
| 微孔表面積(m2/g) | 677.97 | 609.58 | 504.34 |
| 外部面積(m2/g) | 128.94 | 113.30 | 287.01 |
| 微孔表面積占比(%) | 84.02 | 84.33 | 63.73 |
| 總孔隙體積(cm3/g) | 0.43 | 0.39 | 0.52 |
| 微孔體積(cm3/g) | 0.36 | 0.32 | 0.27 |
| 微孔體積占比(%) | 83.28 | 82.12 | 51.37 |
| 平均孔徑(Å) | 21.19 | 21.59 | 26.50 |
3.2.3 掃描式電子顯微鏡分析
利用掃描式電子顯微鏡(Scanning Electron Microscope, SEM)和X射線能量散布分析儀(Energy-dispersive X-ray spectroscopy, EDS),可以觀察並分析活性碳的表面形態特徵以及元素分析。SEM結果如 圖5所示,放大倍率分別為500倍及1000倍。活性碳A和MU由圖中可以明顯的觀察到兩者的表面構造類似,這可能與兩者皆為椰子殼的原料來源有關 ; 活性碳F400的表面較其餘兩者粗糙不規則,並呈現蜂巢狀,而其來源為煙煤。EDS分析結果,三種活性碳皆由元素C構成,無其他元素參雜。
圖5、三種GAC之SEM觀測

3.3 活性碳吸附試驗與挑選
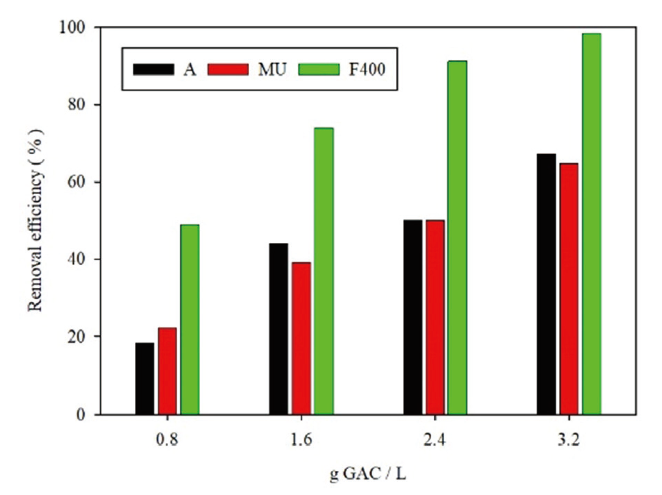
由實驗室以市售PFBS藥品(97%, Sigma-Aldrich)配置濃度同為200mg/L之標準溶液,利用三種GAC以不同條件分別測試去除效果,以對其吸附機制進一步探討與釐清,圖6為三種不同廠牌之GAC碳液比對目標污染物PFBS的去除率變化情形,由此可知,隨著反應時間越長,每單位碳量越高,則對PFBS的去除效果越好,此現象應與反應接觸的比表面積較大,導致同樣擁有較大的總可吸收量有關。以 圖7中將三種GAC吸附6小時後的PFBS去除率相互比較後,可以發現F400型之去除效果明顯較佳,可達98.46%,其次依序為A(67.24%)和MU(64.69%)。
圖6、四種碳液比下GAC對PFBS去除率之變化情形 ([PFBS]0=200mg/L, pH=3, Stirring speed=550rpm, Temp.=25°C)
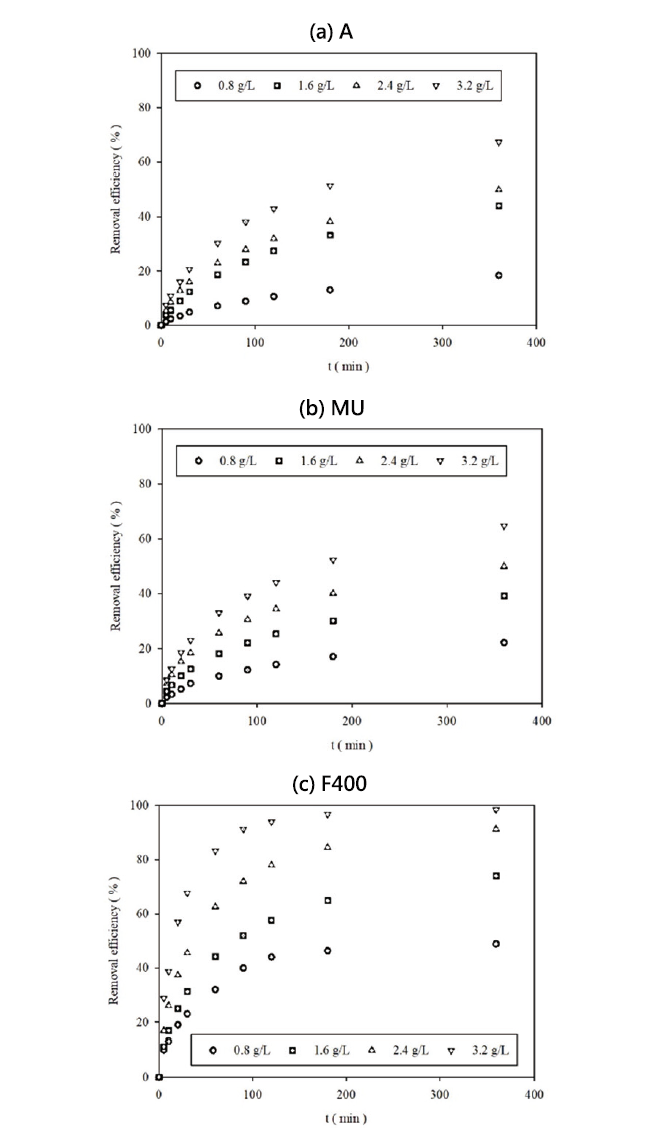
圖7、吸附6小時後三種GAC對PFBS之去除率比較 ([PFBS]0=200mg/L, pH=3, Stirring speed=550rpm, Temp.=25°C, Time=6hr)
針對GAC吸附PFBS達吸附平衡所需的最短時間,經初步的實驗結果約為2,880分鐘,即2天。由 圖8可知,在360分鐘以前去除率以及吸附量會快速上升,之後吸附速率便趨緩,推論因為一開始時活性碳與溶液間的濃度梯度最大,吸附速率最快,隨著吸附量上升,吸附速率會隨濃度梯度下降而越來越小並趨近於吸附平衡,達到最終穩定的濃度,以到終點時的吸附能力來看,去除率和吸附量由高至低為F400>A>MU。此外,圖中皆顯示去除率會隨著環境pH值提高而下降,乃PFBS的pKa為0.14,在溶液中為陰離子團之解離型態,而 圖2顯示在pH為3時三種活性碳為帶正電或最接近零電位點,因此去除率最高,隨著pH值上升,活性碳表面負電壓越大,PFBS和活性碳之間的靜電排斥力越大,因此去除率隨著pH值上升而下降,進而證實前述3.1.1章節之理論。另於去除率最高的pH為3環境下,在反應開始後分時段個別量測三種GAC的去除率和吸附量,紀錄如 圖9,可知去除率和吸附量由高至低的表現同為F400>A>MU。各項結果皆顯示F400型GAC對於去除水中PFBS比起其於兩者有顯著之成效差異,故於實廠驗證階段,本研究將選定原料為煙煤的F400型GAC,作為實廠廢水連續運轉的測試材料。
圖8、四種pH下GAC對PFBS去除率之變化情形 ([PFBS]0=200mg/L, 3.2g/L GAC, Stirring speed=550rpm, Temp.=25°C)
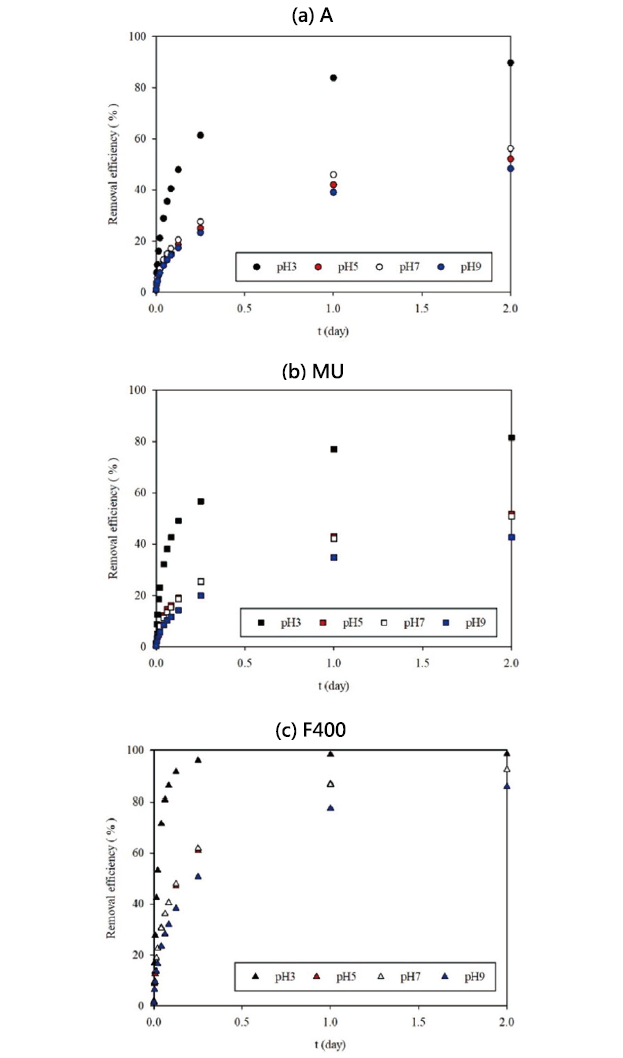
圖9、比較酸性條件(pH=3)下三種GAC的(a)去除率及(b)吸附率隨時間之變化 ([PFBS]0=200mg/L, 3.2g/L GAC, pH=3, Stirring speed=550rpm, Temp.=25°C)

4. 實廠測試驗證
前述材質分析得知F400型活性碳擁有最佳PFBS去除表現,今設計並建置一連續式操作活性碳吸附塔(GAC Filter),內部填充F400型活性碳,依據3.3章節所得結果,以停留時間2天為設計,做晶圓廠實際廢水處理測試。實廠廢水中存在的短碳鏈全氟化合物,為數種結構類似PFBS之磺胺化合物混合型態,包含PFBS衍生物及鹽類(以PFBSx簡稱此混合物)。然而並非所有廢水皆含PFBSx,根據不同廢水水質特性,廠內將不同種類廢水分類,以專管蒐集,由源頭製程機台端將廢水排放至相對應的水處理系統,藉以達到高水回收率與精準處理。
盤點工廠內使用的化學品,並檢測機台使用後排放廢水中的PFBSx含量,發現約有五種的化學藥劑,其中包含顯影液或研磨液等含有相關成份,分析濃度並換算放流廢水中質量占比,主要貢獻來自於晶圓製造環節中的黃光製程。黃光製程廢水含四甲基氫氧化銨(Tetramethyl ammonium hydroxide, TMAH),九成以上排至其專屬的廢水專管(TMAH Drain),分區收集後集中至TMAH廢水處理系統,以串聯二段的陽離子樹脂塔,由吸附方式將廢水中的TMAH攔截,所得乾淨產水作為次級回收水使用,而樹脂再生廢液則出廠重製再利用。本研究規劃於TMAH廢水處理系統中再串聯兩套活性碳塔吸附PFBSx,理論上可以攔截九成以上PFBSx。然而,尚餘部分有來自上游化學品供應系統的直接排放,或其它分布於不同類型的廢水排放管,為此本研究另外增設一專門導入本案活性碳塔的廢水專管(SWD Drain),收受其餘游離含微量比例PFBSx的廢水,以求能全數納管入活性碳塔內去除。
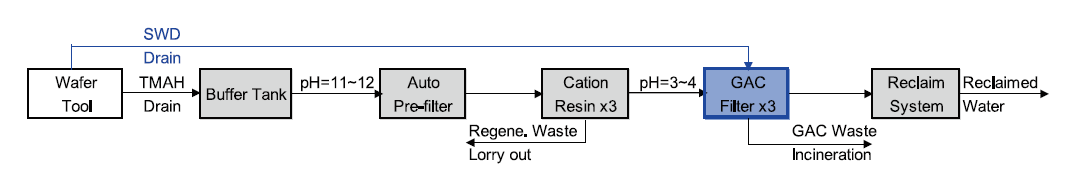
圖10表述本系統處理流程,藍色標示為本研究新增單元,其餘為既設設備。於晶圓製造機台端,將含有PFBSx的廢水專管收集,以陽離子樹脂塔去除TMAH,再於其出口安排串聯的活性碳塔吸附PFBSx。經由此配置,可使原本偏鹼性原水(pH=11~12)經由氫型樹脂作離子交換後,釋放氫離子將pH降至3~4,再進入活性碳塔處理,對應3.1.1及3.2章節研究結果,於pH=3酸性條件下剛好可得到較佳之去除率,使得本配置可不需額外加藥。
圖10、新設TMAH廢水處理系統流程示意圖
4.1 實廠連續式操作取樣
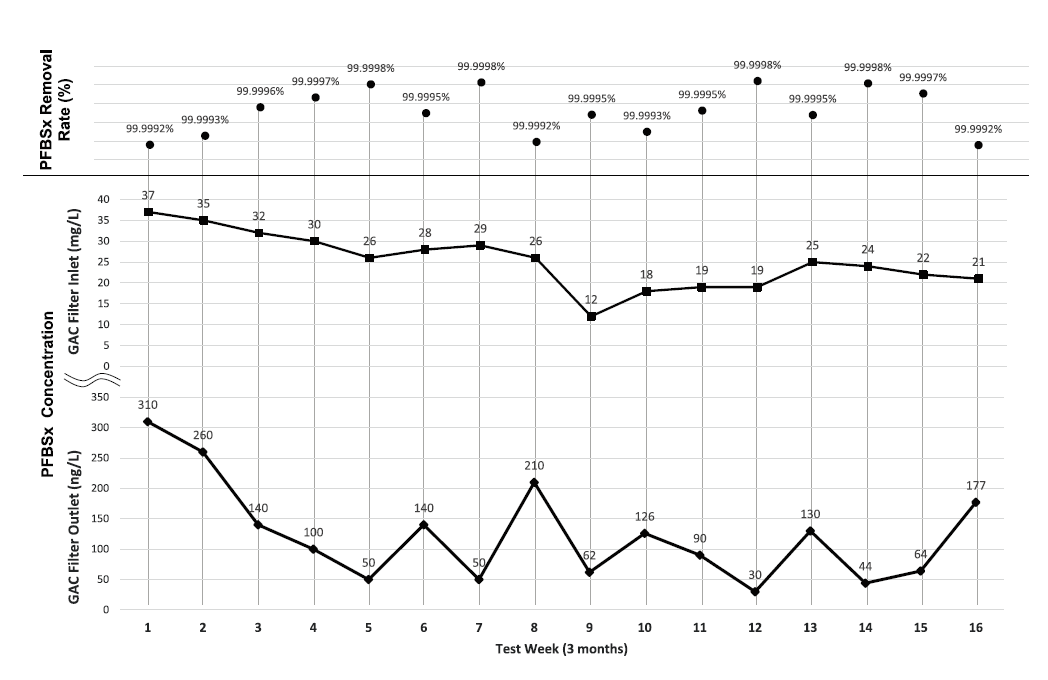
將上述流程建置於一運作中的研發型晶圓廠,並同步增設SWD專管收集系統,以做為母廠(Mother FAB)測試,圖11顯示該廠區系統設置後,進、出口水中PFBSx濃度取樣數值的變化歷程,檢測方式以液相層析串聯質譜儀(Liquid Chromatography Tandem Mass Spectrometer, LC-MS/MS)作定量分析,分別檢測PFBSx內含的所有型態化合物濃度後加總之結果。於三個月的連續追蹤期間,其活性碳在連續式廢水進流操作,無逆洗程序及無更換濾材的情況下,仍具有穩定的PFBSx去除效果,且去除率皆有達到99.9992%以上(平均99.9995%),將原本濃度為12至37mg/L(ppm)等級,在出水端降解至30~310ng/L(ppt)等級,由此可知以活性碳吸附法對短碳鏈的全氟化合物,為有效可靠的解決辦法,並且吸附材的吸附能力可穩定達三個月以上無需更換,為避免交叉污染亦不設定逆洗程序,增設此單元額外衍生的人力負擔並不顯著。
圖11、晶圓廠以F400型活性碳處理之入/出水PFBSx濃度取樣結果
4.2 多廠放流水去除效果驗證
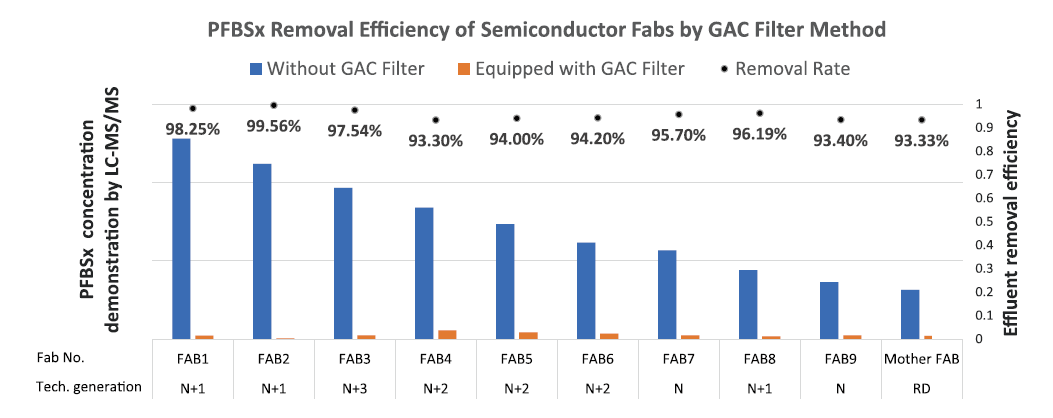
前述母廠試驗成功後,將同樣系統配置複製至其他九個生產型晶圓廠,其追蹤結果如 圖12所示。本試驗於導入前後,分別以同樣LC-MS/MS定量分析檢測放流水PFBSx總含量,參與試驗的各個晶圓廠彼此半導體製程級距橫跨四個世代,包含涵蓋水質變動較大的研發(Research & Development, RD)母廠,各廠所使用之化學品、水質條件及廢水回收系統設計隨世代約略不同,但於導入前的放流水質檢測,同時都檢測出含有少量PFBSx物質。經由本研究之活性碳塔與SWD專管設置後,圖12顯示設置前後為期一個月的連續取樣結果平均值,放流水的PFBSx改善率不論製程世代各有不同,卻皆能達到93.3%~98.3%(平均95.55%)不等的高去除效果,測試期間設備運轉表現亦穩定,證實本方法可廣泛在半導體產業中投入使用,短碳鏈全氟化合物問題因此得以明顯改善。
圖12、不同世代晶圓廠放流水PFBSx削減成效與去除率

4.3 廢碳清運與焚化
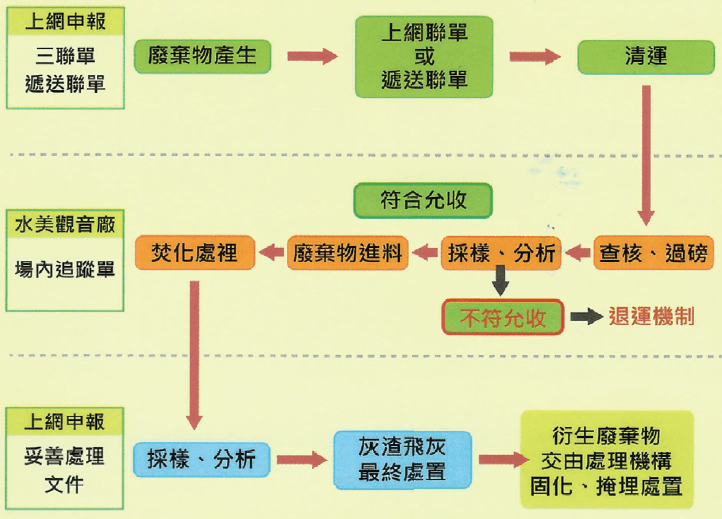
針對達吸附終點之GAC,本案另規劃完善處理程序將塔內活性碳汰舊換新,包含設計備塔運轉(N+1)實現不間斷的廢水處理,施工程序首先由廠務端廢水專責人員於線上追蹤系統開立預防性保養施工單,遂由合約承攬商將待命塔內的廢碳完整抽出,現場確認施作成果後放行填入新碳。同時,如圖13所示,產生的廢碳由廠內廢棄物專責人員依法申報開立聯單,安排合法清運及處理業者依照「廢棄物允收準則」進行必要之採樣檢測管理後,透過秤重、混摻進料、旋轉窯焚化與二次燃燒等多道程序,以高溫分解廢碳中之全氟化合物,並藉由其專業之尾氣處理設備過濾排氣與飛灰,並配有即時空污監測杜絕環境污染。於此,得於宏觀條件下完備本案之全氟化合物實質削減策略。
圖13、GAC廢碳清運與焚化處理流程
5. 結論
本研究分析不同的全氟化合物處理方法,經由多方文獻比較,選定顆粒活性碳吸附法為晶圓製造業最適方法,並藉由實驗發現,原料為煙煤的活性碳,在pH<3.73的酸性條件因表面帶正電擁有較高的PFBS去除效果。將前述結論建置實廠化試驗模組,同步分析廢水來源,並配置短碳鏈全氟化合物之混合物(PFBSx)廢水專管,以連續式進流處理,發現系統端PFBSx去除率可長期穩定達99.9%以上。於多廠的模組複製驗證結果顯示,各廠放流水PFBSx改善率亦可達93.3%以上,成果顯著具代表性,確認實務上本方法為可靠且穩定的策略措施。
觀察放流端平均改善率95.55%較GAC出口平均去除率99.9995%稍低之現象,推測本試驗即便將大多數含PFBSx廢水收集於SWD與TMAH drain,但仍有極少比例的游離PFBSx流佈於其他種drain類別,顯示製程機台端的分流精確度,於未來仍具改善空間。
參考文獻
- Boulanger, B., Vargo, J.D., Schnoor, J.L. and Hornbuckle, K.C., 2005. Evaluation of perfluorooctane surfactants in a wastewater treatment system and in a commercial surface protection product. Environmental Science & Technology. 39(15), 5524-5530.
- Fletcher, T., 2011. Monitoring the Health of Populations With Polluted Drinking Water. The Example of Perfluorinated Compounds. Epidemiology. 22(1), S58-S58.
- Lin, Y.-C., Lai, W.W.-P., Tung, H.-h. and Lin, A.Y.-C., 2015. Occurrence of pharmaceuticals, hormones, and perfluorinated compounds in groundwater in Taiwan. Environmental Monitoring and Assessment. 187(5).
- Zhao, Z., Cheng, X., Hua, X., Jiang, B., Tian, C., Tang, J., Li, Q., Sun, H., Lin, T., Liao, Y. and Zhang, G., 2020. Emerging and legacy per- and polyfluoroalkyl substances in water, sediment, and air of the Bohai Sea and its surrounding rivers. Environmental Pollution. 263.
- Moeller, A., Ahrens, L., Surm, R., Westerveld, J., van der Wielen, F., Ebinghaus, R. and de Voogt, P., 2010. Distribution and sources of polyfluoroalkyl substances (PFAS) in the River Rhine watershed. Environmental Pollution. 158(10), 3243-3250.
- Jian, J.-M., Chen, D., Han, F.-J., Guo, Y., Zeng, L., Lu, X. and Wang, F., 2018. A short review on human exposure to and tissue distribution of per- and polyfluoroalkyl substances (PFASs). Science of the Total Environment. 636, 1058-1069.
- Haug, L.S., Thomsen, C., Brantsaeter, A.L., Kvalem, H.E., Haugen, M., Becher, G., Alexander, J., Meltzer, H.M. and Knutsen, H.K., 2010. Diet and particularly seafood are major sources of perfluorinated compounds in humans. Environment International. 36(7), 772-778.
- Olsen, G.W., Burris, J.M., Ehresman, D.J., Froehlich, J.W., Seacat, A.M., Butenhoff, J.L. and Zobel, L.R., 2007. Half-life of serum elimination of perfluorooctanesulfonate, perfluorohexanesulfonate, and perfluorooctanoate in retired fluorochemical production workers. Environmental Health Perspectives. 115(9), 1298-1305.
- Dong, G.-H., Tung, K.-Y., Tsai, C.-H., Liu, M.-M., Wang, D., Liu, W., Jin, Y.-H., Hsieh, W.-S., Lee, Y.L. and Chen, P.-C., 2013. Serum Polyfluoroalkyl Concentrations, Asthma Outcomes, and Immunological Markers in a Case-Control Study of Taiwanese Children. Environmental Health Perspectives. 121(4), 507-513.
- Hoffman, K., Webster, T.F., Weisskopf, M.G., Weinberg, J. and Vieira, V.M., 2010. Exposure to Polyfluoroalkyl Chemicals and Attention Deficit/Hyperactivity Disorder in U.S. Children 12-15 Years of Age. Environmental Health Perspectives. 118(12), 1762-1767.
- Gewurtz, S.B., Bradley, L.E., Backus, S., Dove, A., McGoldrick, D., Hung, H. and Dryfhout-Clark, H., 2019. Perfluoroalkyl Acids in Great Lakes Precipitation and Surface Water (2006-2018). Environmental Science & Technology. 53(15), 8543-8552.
- Li, F., Duan, J., Tian, S., Ji, H., Zhu, Y., Wei, Z. and Zhao, D., 2020. Short-chain per- and polyfluoroalkyl substances in aquatic systems: Occurrence, impacts and treatment. Chemical Engineering Journal. 380.
- Brendel, S., Fetter, E., Staude, C., Vierke, L. and Biegel-Engler, A., 2018. Short-chain perfluoroalkyl acids: environmental concerns and a regulatory strategy under REACH. Environmental Sciences Europe. 30.
- Cai, M., Zhao, Z., Yin, Z., Ahrens, L., Huang, P., Cai, M., Yang, H., He, J., Sturm, R., Ebinghaus, R. and Xie, Z., 2012. Occurrence of Perfluoroalkyl Compounds in Surface Waters from the North Pacific to the Arctic Ocean. Environmental Science & Technology. 46(2), 661-668.
- Zhao, P., Xia, X., Dong, J., Xia, N., Jiang, X., Li, Y. and Zhu, Y., 2016. Short- and long-chain perfluoroalkyl substances in the water, suspended particulate matter, and surface sediment of a turbid river. Science of the Total Environment. 568, 57-65.
- Jeong, J., Song, W.H., Cooper, W.J., Jung, J. and Greaves, J., 2010. Degradation of tetracycline antibiotics: Mechanisms and kinetic studies for advanced oxidation/reduction processes. Chemosphere. 78(5), 533-540.
- Bao, Y., Deng, S., Jiang, X., Qu, Y., He, Y., Liu, L., Chai, Q., Mumtaz, M., Huang, J., Cagnetta, G. and Yu, G., 2018. Degradation of PFOA Substitute: GenX (HFPO-DA Ammonium Salt): Oxidation with UV/Persulfate or Reduction with UV/Sulfite? Environ Sci Technol. 52(20), 11728-11734.
- Yang, L., He, L.Y., Xue, J.M., Ma, Y.F., Shi, Y., Wu, L. and Zhang, Z.L., 2020. UV/SO 3 2? based advanced reduction processes of aqueous contaminants: Current status and prospects. Chemical Engineering Journal. 397.
- Bentel, M.J., Yu, Y.C., Xu, L.H., Li, Z., Wong, B.M., Men, Y.J. and Liu, J.Y., 2019. Defluorination of Per- and Polyfluoroalkyl Substances (PFASs) with Hydrated Electrons: Structural Dependence and Implications to PFAS Remediation and Management. Environmental Science & Technology. 53(7), 3718-3728.
- Sun, M., Zhou, H., Xu, B. and Bao, J.X., 2018. Distribution of perfluorinated compounds in drinking water treatment plant and reductive degradation by UV/SO32- process. Environmental Science and Pollution Research. 25(8), 7443-7453.
- Banks, D., Jun, B.M., Heo, J., Her, N., Park, C.M. and Yoon, Y., 2020. Selected advanced water treatment technologies for perfluoroalkyl and polyfluoroalkyl substances: A review. Separation and Purification Technology. 231.
- Tang, C.Y.Y., Fu, Q.S., Robertson, A.P., Criddle, C.S. and Leckie, J.O., 2006. Use of reverse osmosis membranes to remove perfluorooctane sulfonate (PFOS) from semiconductor wastewater. Environmental Science & Technology. 40(23), 7343-7349.
- Appleman, T.D., Dickenson, E.R.V., Bellona, C. and Higgins, C.P., 2013. Nanofiltration and granular activated carbon treatment of perfluoroalkyl acids. Journal of Hazardous Materials. 260, 740-746.
- Taniyasu, S., Yamashita, N., Yamazaki, E., Petrick, G. and Kannan, K., 2013. The environmental photolysis of perfluorooctanesulfonate, perfluorooctanoate, and related fluorochemicals. Chemosphere. 90(5), 1686-1692.
- Cao, M.H., Wang, B.B., Yu, H.S., Wang, L.L., Yuan, S.H. and Chen, J., 2010. Photochemical decomposition of perfluorooctanoic acid in aqueous periodate with VUV and UV light irradiation. Journal of Hazardous Materials. 179(1-3), 1143-1146.
- Ribao, P., Rivero, M.J. and Ortiz, I., 2017. TiO2 structures doped with noble metals and/or graphene oxide to improve the photocatalytic degradation of dichloroacetic acid. Environmental Science and Pollution Research. 24(14), 12628-12637.
- Gomez-Ruiz, B., Ribao, P., Diban, N., Rivero, M.J., Ortiz, I. and Urtiaga, A., 2018. Photocatalytic degradation and mineralization of perfluorooctanoic acid (PFOA) using a composite TiO2 -rGO catalyst. Journal of Hazardous Materials. 344, 950-957.
- Niu, J.F., Li, Y., Shang, E.X., Xu, Z.S. and Liu, J.Z., 2016. Electrochemical oxidation of perfluorinated compounds in water. Chemosphere. 146, 526-538.
- Schaefer, C.E., Andaya, C., Burant, A., Condee, C.W., Urtiaga, A., Strathmann, T.J. and Higgins, C.P., 2017. Electrochemical treatment of perfluorooctanoic acid and perfluorooctane sulfonate: Insights into mechanisms and application to groundwater treatment. Chemical Engineering Journal. 317, 424-432.
- Liao, Z.H. and Farrell, J., 2009. Electrochemical oxidation of perfluorobutane sulfonate using boron-doped diamond film electrodes. Journal of Applied Electrochemistry. 39(10), 1993-1999.
- Vecitis, C.D., Park, H., Cheng, J., Mader, B.T. and Hoffmann, M.R., 2008. Kinetics and mechanism of the sonolytic conversion of the aqueous perfluorinated surfactants, perfluorooctanoate (PFOA), and perfluorooctane sulfonate (PFOS) into inorganic products. Journal of Physical Chemistry A. 112(18), 4261-4270.
- Vecitis, C.D., Wang, Y.J., Cheng, J., Park, H., Mader, B.T. and Hoffmann, M.R., 2010. Sonochemical Degradation of Perfluorooctanesulfonate in Aqueous Film-Forming Foams. Environmental Science & Technology. 44(1), 432-438.
- Du, Z.W., Deng, S.B., Bei, Y., Huang, Q., Wang, B., Huang, J. and Yu, G., 2014. Adsorption behavior and mechanism of perfluorinated compounds on various adsorbents-A review. Journal of Hazardous Materials. 274, 443-454.
- Fujii, S., Polprasert, C., Tanaka, S., Lien, N.P.H. and Qiu, Y., 2007. New POPs in the water environment: distribution, bioaccumulation and treatment of perfluorinated compounds - a review paper. Journal of Water Supply Research and Technology-Aqua. 56(5), 313-326.
- Schroder, H.F., Jose, H.J., Gebhardt, W., Moreira, R. and Pinnekamp, J., 2010. Biological wastewater treatment followed by physicochemical treatment for the removal of fluorinated surfactants. Water Science and Technology. 61(12), 3208-3215.
- Ochoa-Herrera, V. and Sierra-Alvarez, R., 2008. Removal of perfluorinated surfactants by sorption onto granular activated carbon, zeolite and sludge. Chemosphere. 72(10), 1588-1593.
- Carter, K.E. and Farrell, J., 2010. Removal of Perfluorooctane and Perfluorobutane Sulfonate from Water via Carbon Adsorption and Ion Exchange. Separation Science and Technology. 45(6), 762-767.
- Schröder, H.F., José, H.J., Gebhardt, W., Moreira, R.F.P.M. and Pinnekamp, J., 2010. Biological wastewater treatment followed by physicochemical treatment for the removal of fluorinated surfactants. Water Science and Technology. 61(12), 3208-3215.


留言(0)