摘要
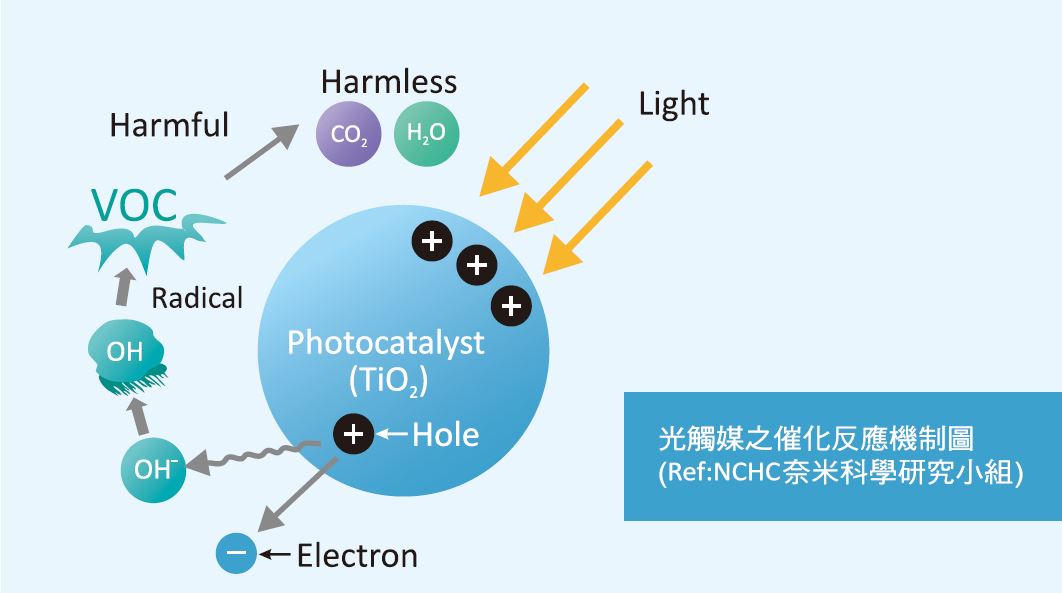
利用光觸媒對氣態甲苯在含有 TiO2 超音波微霧粒環境下降解之探討 - 不需消耗太多的能源
Keywords / Volatile Organic Compounds10,Utrasonic Mist,Photocatalyst Particles
本研究將凝態的 TiO2 利用超音波原子化器轉換成微霧滴,在不同的條件下對氣態甲苯的光觸媒降解之研究,在 365nm 的 UV 光輻射下,甲苯在光觸媒 TiO2 微霧滴的表面及裡面進行解離及礦物化。甲苯的去除效率隨著TiO2 微霧滴的濃度增加而增加,在 254nm+185nm 光輻射下,礦物化 (mineralization) 比率比在 365nm 光輻射下高,甲苯在 254nm+185nm 光輻射下及在 O3 氧化劑存在時立即光解轉換成親水性化合物,中間物在媒TiO2 微霧滴被擄獲而礦物化轉成 CO 及 CO2,本論文即對超音波微霧粒及 TiO2 光觸媒有效利用率進行探討。
緒論
在室內空間存在不同型態的氣體污染物,藉由利用臭氧氧化劑及TiO2,光觸媒對空氣污染物已有人研究[1-5],雖然有效分解有機污染物如揮發性有機污染物(volatile organic compounds, VOC)降解至CO及CO2等技術,此技術也有些難題,例如溼度對高去除效率的影響及親水性中間物的產率與降解產物的關係等問題[6]。超音波原子化產生直徑比10μm還小的超精細液滴的技術是有用的[7,8],此技術與加熱法或使用輻射法比較,不需太多的消耗能源即可達到去除效果[9]。
本研究TiO2光觸媒顆粒以超音波原子化器轉換成微霧滴,在相對穩定的溼度下,對光觸媒降解污染物及捕獲親水性中間物有效率的達到去除效果。此超音波微霧粒(utrasonic mist, UM內 )內含光觸媒顆粒(photocatalyst particles)亦稱為UMP。對VOC去除效率以申苯為例,甲苯利用UMP法對光觸媒降解及礦物化現象達到有效去除之研究是本研究探討主要的研究議題。
PERIMENT 實驗設備
以UMP法對TiO2顆粒的探討
UMP法利用超音波震盪器(HM-303N, Honda Electron Co.)在室溫下 TiO2 加入500mL水於塑膠杯中農溫,再用重力沉澱法在鋁箔紙上收集UMP,TiO2 顆粒在50°C乾燥0.5小時再利用SEM觀察其表面性質,不同濃度containing 0.10、0.50、1.0、及 1.5gL-1 的TiO2 ,觀察其產生微霧滴的大小。
甲苯降解實驗
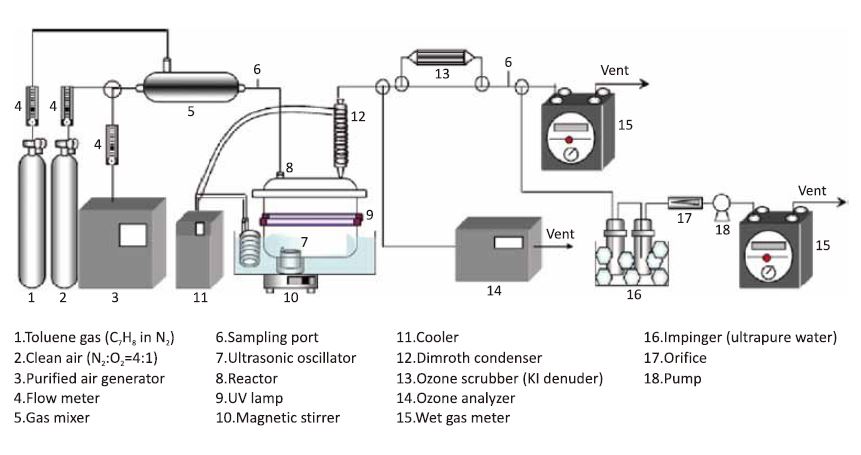
實驗的安装圖如圖一所示,雙管UV管放置反應器內,2.4-MHz超音波震盪器是放置於反應器底部,本研究將以兩中型態的UV燈管進行探討。(1)4W黑光藍燈〔black light blue(BLB)Lamp〕輻射強度為365nm。(2)4WGL24 臭氧燈具有185nm及254nm兩種中放射光源。
圖一、Schematic of apparatus used for photocatalytic reaction in the ultrasonic mist
Degussa P25 TiO2 光觸媒取自Nippon Aerosil公司,內含80%anatase型及20%rutle型,平均顆粒大小為21nm,顆粒表面積為50m2g-1。
以甲苯標準氣體(42.6ppm/N2,Takachiho Chemical Industrial Co.Ltd.),稀釋成0.6及4.0ppm,以氣體流速1L / min 進入反應器,0.6 ppm甲苯分別在0、0.01、0.05及1.0g/LTiO2環境下,探討甲苯的去除效率。
UMP大小分佈測試及分析
霧滴大小分佈使用低體積空氣取樣器(Tokyo Dylec, AN-200),收集流速及時間為16.7L/min及2min。臭氧濃度使用UV吸收臭氧分析儀(Shimadzu, UVAD-1000),甲苯濃度利用氣相層析火焰離子偵測器量測(GC-FID;Shimadzu,GC-7A),礦物化解離產物為CO及CO2以GC-FID測試。
TIONS / DICUSSION 問題與討論
在 UM 中 TiO2 顆粒的 SEM 測試
在超音波霧滴(UM)中確認TiO2顆粒的存在,收集及乾燥超音波霧滴後測試SEM,如圖二所示,由SEM影像顯示在超音波霧滴中TiO2顆粒分佈狀態,當超音波霧滴顆粒照UV燈後在其表面誘導光觸媒進行反應。
圖二、SEM images of collected and dried UMP generated from slurries containing (a) 0.10 g L-1, (b) 0.50 g L-1, and (c) 1.0 g L-1, of TiO2

甲苯去除
光觸媒
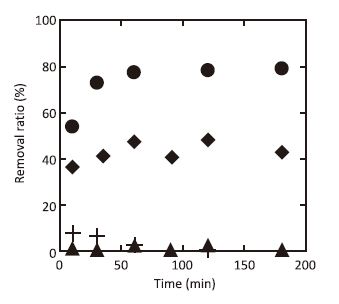
超音波霧滴產生在只有 ultrasonic(US)、US/TiO2、UV365/TiO2及US/UV365等四條件下,對甲苯的去除效率與時間作圖如圖三所示,在只有US及US/TiO2 環境下,甲苯的去除效率為無反應,因甲苯的疏水性在此條件下超音波霧滴及TiO2超音波霧滴顆粒無法捕獲甲苯進行反應。
圖三、Comparison of toluene removal ratios for the following reaction conditions : (●)US/UV365/TiO2, (▲)US, (♦)UV365/TiO2, and (+) US/TiO2. Toluene concentration, 0.60ppm; gas flow rate, 1.0 L min-1 ; TiO2 amount, 1.0 g L-1.
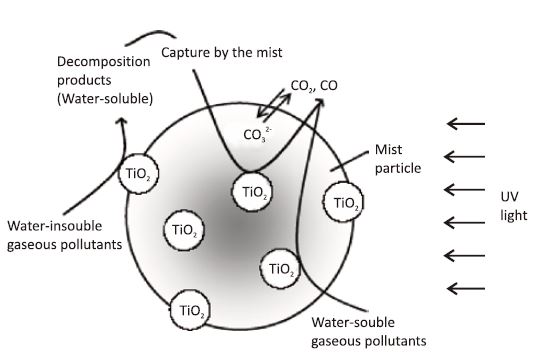
當甲苯在 UV365/TiO2及and US/UV365 環境下,甲苯在氣、液相接觸面進行光觸媒反應,甲苯開始降解,在液相中TiO2顆粒被充份分布在氣-液相的表面,藉由TiO2光觸媒反應產生不穩定產物,如OH自由基不僅在TiO2產生,而且在氣相接近液相地方亦會產生,在氣相中TiO2表面不穩定產物的放射已有很多論文被報導[10,11],另外在 US/UV365/TiO2 條件下,因甲苯在超音波霧滴顆粒表面被光觸媒有效的降解,使超音波霧滴顆粒的TiO2被分布在氣-液的介面上,之後,在霧滴表面藉由光觸媒反應於超音波霧滴顆粒產生親水性的中間產物。當實驗在0.6ppm甲苯中間產物不斷的被降解成CO及CO2,在反應器的中間產物是無法被偵測的,反應機構如圖四所示。
圖四、Degradation mechanism for gaseous pollutants in the mist
觸媒質量對甲苯去除效率之影響
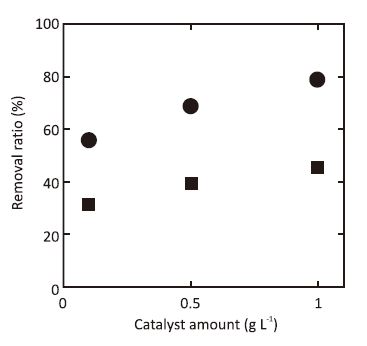
觸媒質量變化對UMP產出及氣體污染物的去除是重要因素,觸媒質量對甲苯去除效率之影響如圖五所示。
圖五、Dependence of toluene removal ratio on catalyst amount for the following reaction conditions: (●) US/UV365 / TiO2, and (∎) UV365/TiO2, Toluene concentration, 0.60ppm; gas flow rate, 1.0 L min-1; Tio2, concentration, 1.0 g L-1; UV wavelength, 365nm.
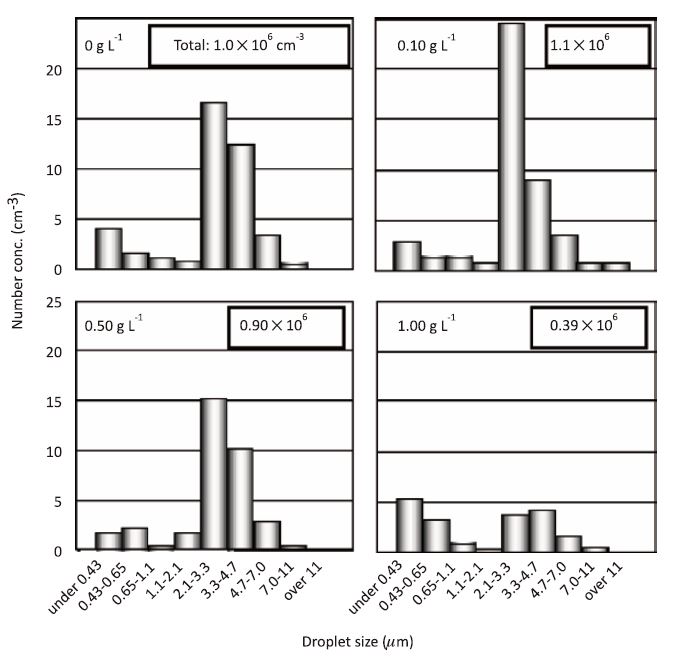
在UMP中不同TiO2濃度0、0.10、0.50、1.0、及1.5gL-1 對顆粒大小的分布影響,如圖六所示,主要的顆粒大小在2.1~3.3μm,此值與論文所報導過的數值相近[7]。
圖六、Comparison of droplet size number concentrations for various TiO2 catalyst amounts.
由圖五中所示,甲苯去除效率隨觸媒TiO2量的增加而增加,隨觸媒TiO2顆粒直徑增加而減少,由上述可得到幾點結論:
(1)觸媒活性隨觸媒TiO2,量增加而增加。
(2)UV光遷移隨著超音波遷移减小而增加[12-15]。
UV波長效率
UV光效率對甲苯去除及礦物化之研究結果,如表1所示,對UV365及UV185+254兩道UV光降解機制有所不同,在UV365幅射下,光觸媒反應機制在超音波霧滴顆粒的TiO2表面發生反應,相反地,在UV185+254幅射下,從空氣中的O2產生O3,O3為強氧化劑,並由水氣中的解離產生OH而直接參與觸媒反應,此反應O3及OH在氣相中攻擊甲苯立即轉換成CO及CO2或成親水性降解化合物,親水性降解化合物在超音波霧滴顆粒的TiO2上具有高度的反應,因此在UV185+254幅射下對甲苯的去除效率比UV365高,不僅是甲苯的降解如此效率,甲苯的礦物化現象亦是如此。
CONCLUSION 結論
本研究是由TiO2的泥漿中藉由超音波震盪出小霧滴後進行光觸媒降解反應,TiO2的量及UV波長對甲苯降解的影響進行研究,可得到下列幾點結論:
- 甲苯藉產生超音波霧滴顆粒的TiO2的光反應轉換成親水性中間物,將甲苯去除。
- 甲苯的去除效率隨著TiO2量增加而增加。
- 甲苯的去除及礦物化效率於在UV185+254比在UV365效果好,因甲苯在具有O3及OH ‧ 的環境下,將轉換成CO及CO2或成親水性降解化合物。
- 本研究結果使用超音波霧滴顆粒的TiO2參與光解,將有效去除甲苯,為低成本有用的去除空氣污染技術。
參考文獻
- J.Y. Jeong, K. Sekiguchi, K. Sakamoto, Chemosphere 57 (2004) 663.
- K.M. Parida, S.S. Dash, D.P. Das, Journal of Colloid and Interface Science 298 (2006) 787.
- G.M. Zuo, Z.X. Cheng, H. Chen, G.W. Li, T. Miao, Journal of Hazardous Materials B 128 (2006) 158.
- A. Nakajima, H. Obata, Y. Kameshima, K. Okada, Catalysis Communications 6 (2005) 716.
- F. Bosc, D. Edwards, N. Keller, V. Keller, A. Ayral, Thin Solid Films 495 (2006) 272.
- J.Y. Jeong, K. Sekiguchi, W.K. Lee, K. Sakamoto, Journal of Photochemistry and Photobiology A: Chemistry 169 (2005) 279.
- R.J. Lang, The Journal of the Acoustical Society of America 34 (1962) 6.
- T.D. Donnelly, J. Hogan, A. Mugler, M. Schubmehl, N. Schommer, Review of Scientific Instruments 76 (2005) 1.
- W.R. Wood, A.L. Loomis, The London, Edinburgh, and Dublin Philosophical Magazine and Journal of Sci-ence 4 (1927) 417.
- T. Tatsuma, S. Tachibana, T. Miwa, D.A. Tryk, A. Fujishima, Journal of Physical Chemistry B 103 (1999) 8033.
- T. Tatsuma, S. Tachibana, A. Fujishima, Journal of Physical Chemistry B 105 (2001) 6987.
- D.M. Kirpalani, F. Toll, Journal of Chemical Physics 117 (2002) 3874.
- K. Suzuki, D.M. Kirpalani, T.W. McCracken, Chemical Engineering and Technology 29 (2006) 44.
- J.M. Meacham, M.J. Varady, F.L. Degertekin, A.G. Fedorov, Physics of Fluids 17 (2005) 1.
- Y. Kawase, T. Masuya, K. Yasuda, M. Nakamura, Journal of Chemical Engineering of Japan 39 (2006) 334.


留言(0)