摘要

半導體廠鹼性廢水的回收與資源再利用技術
Keywords / Membrane Degasifier3,Ammonia Nitrogen,Ammonium Sulfate5,Wastewater Reclaim
含氨 (Ammonia) 的鹼性廢水是半導體廠棘手的問題,因為水中除了氨外,往往還伴隨著高濃度的雙氧水。以回收的方式來濃縮廢水中的氨,並導入脫氣膜 (Membrane Degasifier) 與硫酸反應生成硫酸氨。硫酸氨可再回收當成工業化產品使用,或再製成氨水及其它工業原料。
前言
半導體廠的鹼性排放廢水常含有高濃度的氨與雙氧水,具有污染濃度高、生物毒性高等特性。隨著目前政府所新訂定的放流水總氮濃度,既有廠區須小於20 mg/l,新設廠區須小於10 mg/l的規定即將實施,因此含氨氮廢水的處理是台灣各半導體公司刻不容緩所需面對的。
面對廢水處理問題,最好的處理方法就是回收處理。公司高度重視各廠區的節水問題,與長期合作的協力商發展出一套以回收為前題的氨氮處理技術,它不僅可以克服鹼性廢水中高濃度的H2O2所造成的氧化破壞問題,並可將廢水中的氨去除,回收後的廢水可供廠內次級用水或製程使用。回收水過程中分離濃縮所獲得的高濃度含氨化合物,可以進一步於廠外濃縮精製變成21%的氨水回收再利用,達到最大程度的綠色處理。
流程介紹
本回收處理系統區分為廠內的水回收系統 圖一與廠外的氨水製造與精製純化系統 圖二。
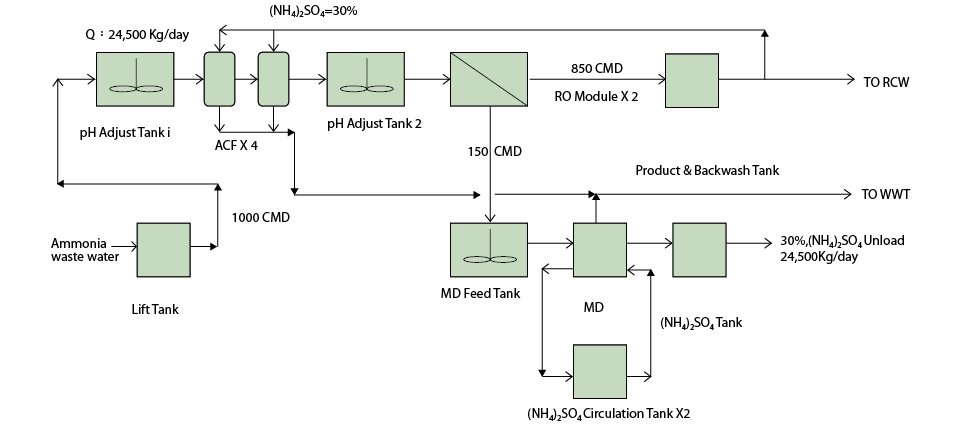
圖一、廠內水回收系統流程圖
圖二、廠外氨水濃縮精製系統流程圖

廠內的水回收處理系統主要包含了以活性碳為主要機制的H2O2去除系統,用以保護後續的處理單元,接著再以逆滲透系統(以下稱RO)去除水中的氨離子及其他的不純物,來進行水的回收,在RO單元中,氨離子被去除並進行初步的濃縮成原來濃度的6-7倍後,此濃縮液再進入非極性的脫氣膜系統(以下稱MD)處理,並進一步的濃縮形成30%的硫酸氨溶液。
廠外的處理單元考量操作的經濟性與產品的品質,我們採用兩階段的處理程序,第一階段先以離子交換將硫酸氨變成氨水(5-11%),第二階段再以超重力蒸餾或真空蒸餾法純化提濃成21%的氨水,供工業用途使用。
系統單元處理機制說明
H2O2系統反應機制說明
由於含氨的鹼性廢水中同時伴隨非常高濃度的H2O2 ( >2,000mg/l ),而接續的回收處理單元,是以薄膜分離為主的處理單元,在有些微的H2O2存在下,薄膜易受氧化破壞,因此H2O2必須預先被去除,才能進入後續的薄膜處理單元。在此我們採用活性碳的催化作用來去除廢水中高濃度的H2O2,以下是活性碳去除H2O2的機制:
雙氧水於鹼性狀態下的鹼催化分解 應 ( base-catalyzed decomposition ) (Weir et al., 1987) 如下式所示:
H2O2+HO2- → H2O+O2+OH- --(2-1)
依據申永順研究(申永順,1992)顯示H2O2單獨系統的穩定性,隨系統溶液pH值增加而降低,此顯示H2O2的穩定性隨HO2-(離子態H2O2)增加而降低。當溶液pH值不進行控制時,溶液pH值會隨反應時間增加而增加,且當溶液pH達12時,亦有H2O2的穩定性隨系統溶液pH值增加而降低的現象,因此(2-1)之反應式是否修正成反應式(2-2),值得進一步探討。本研究後續將配合H2O2消失與OH-產生量進行質量平衡,以確認系統反應機制。
HO2-+HO2-→O2+2OH- ----------(2-2)
AC/ H2O2系統反應機制說明
以活性碳進行H2O2催化的機制包含直接催化(direct catalysis)及間接催化( indirect catalysis),分別說明如下:
直接催化(direct catalysis)
依據Bansal等人(Bansal et al., 1998)之研究顯示,由於活性碳表面的氫氧根離子會與離子態的雙氧水(HO2-)進行交換進而產生過氧化自由基,此自由基會再與雙氧水反應進而產生氧氣,並進一步再生活性碳表面活性位置。
間接催化(indirect catalysis)
Santos等人(Santos, et al., 2009) 、Georgi與 Kopinke(Georgi and Kopinke, 2005)及 Huang等人(Huang et al., 2003)等多位學者大多贊同H2O2與活性碳進行間接催化,也即是活性碳(AC)如Haber-Weiss機制扮演電子傳遞催化劑,如以下二式H2O2在活性碳間接催化下產生OH‧及 HO2‧ 自由基,以進行後續反應。
AC+H2O2 → AC++OH-+OH· ----(2-3)
AC++H2O2 → AC+H++ HO2· ----(2-4)
AC/ H2O2系統預備實驗結果討論
圖三、管柱預備實驗H2O2 去除率與H2O2 成份分佈關係圖
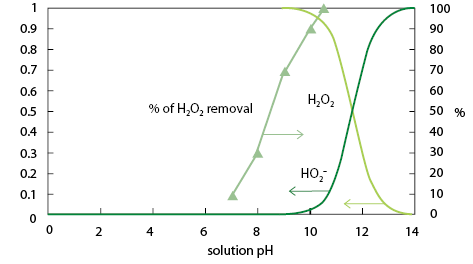
- 由 圖三管柱實驗中得知,H2O2去除率隨溶液pH增加而增加,與以上相關學者關於AC/ H2O2/organics系統中提出H2O2的反應機制均無法有效解釋本研究預備實驗結果,即是AC/ H2O2系統中H2O2的消失速率隨溶液pH值增加而增加。
- 由 圖三管柱實驗中得知,H2O2去除率隨溶液pH增加而增加,其趨勢與離子態H2O2 (HO2-)之成分較具正相關,此結果與Santos等多位學者認同的間接氧化之機制有明顯不同;如能修正Bansal等人提出之直接氧化是經由HO2-與活性碳反應,如此可能較合理解釋實驗結果。
- 由 圖三管柱預備實驗中得知,H2O2去除率隨溶液pH增加而增加,其趨勢雖與離子態H2O2(HO2-)之成分較具正相關,但並非直接相關,是否與活性碳pHzpc(註1)約7~8有關,即當溶液pH大於7時,此時如2-5式H2O2有較大機會與活性碳上的O-進行離子交換,進而產生較多的HO2-,以利於H2O2之去除。
註1. pHzpc : 表面總電荷為零或帶負電時的pH值。
AC-O- + H2O2→ AC-OH + HO2 -----(2-5)
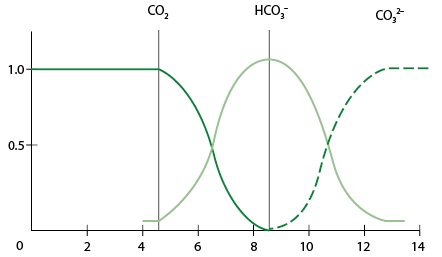
- 批次實驗結果發現,溶液pH越高,氫氧根離子的產生量越高,且氣體的產生量越大。溶液pH=12的AC/ H2O2系統氣體的產生量尤其明顯,氣體可能為CO2及O2,但如 圖四,CO2於pH=12主要以CO32-存在,因此氣體主要為O2。
圖四、CO2 溶於水成分受溶液pH 影響分佈圖
- 根據上述的理論及實驗的結果,我們確認在高pH的溶液條件下,活性碳確實能有效去除H2O2,因此我們將活性碳塔設計在本流程中,並且實證可將廢水中之H2O2從數千mg/l降到趨近於零。
RO Membrane Module 逆滲透系統
利用活性碳將廢水中的H2O2去除後,即可進入RO系統。利用RO來去除水中的氨離子及其他的雜質,一般而言氨在水中呈現的形態與溶液pH有關, 圖五
圖五、NH3 溶於水成分受溶液pH 影響分佈圖(PC-pH Diagram)
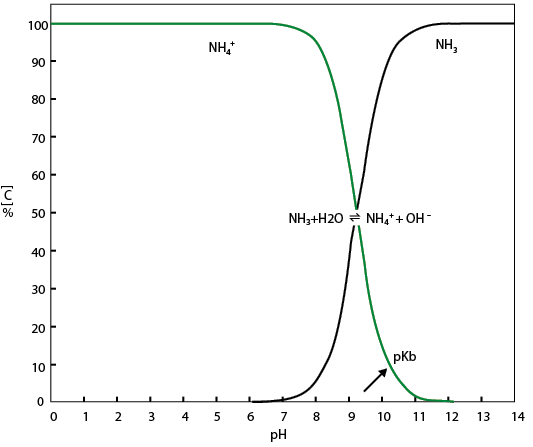
因為在pH較高的情況下,氨是以傾向分子態的形式存在,在分子態的情況下,氣態的氨會造成RO膜氣塞,影響RO的操作,且去除率會隨pH越高而越低。由 圖五我們知道在pH< 6.5的情況下,氨在水中幾乎超過99%是以離子態的形式存在,此時RO膜對水中的氨會有非常好的去除效果。 表一顯示在pH6的溶液條件下RO對Ammonia的去除率>99%,因此RO產水即可回收使用。
|
RO進水PH |
RO進水NH4+ (ppm) |
RO產水NH4+ (ppm) |
RO入口壓力(bar) |
|---|---|---|---|
|
9 |
300-400 |
40 |
16.5 |
|
8 |
300-400 |
16-20 |
16.8 |
|
7 |
300-400 |
3-4 |
17.2 |
|
6 |
300-400 |
0 |
17.5 |
在低pH的操作條件下,水中幾乎所有的氨會被RO去除,而濃縮在RO的濃縮水中,此時的含氨的濃縮水約為原廢水量的1/5,接著我們再利用MD(Membrane Degasifer)以硫酸進一步吸收來進行提濃。
MD脫氣膜系統
經RO將水中的氨離子去除後,RO產水做回收使用,但留在RO濃縮側的氨離子濃度很高,須進一步地將其去除才能符合未來的氨氮放流標準。使用MD來去除水中的氨離子有下列的優點:
- 去除率可高達95%以上。
- 本反應都是在液相中進行反應,不會有氨氣擴散的問題。
- 反應完所產生的硫酸銨,是屬於極安定的物質,環安問題較少。
- 設備所需的空間及面積很小,較適宜半導體廠等空間缺乏的地方。
- 搭配前面的RO系統可將鹼性廢水濃縮成2-3%的硫酸氨溶液,便於後續的外運處理。
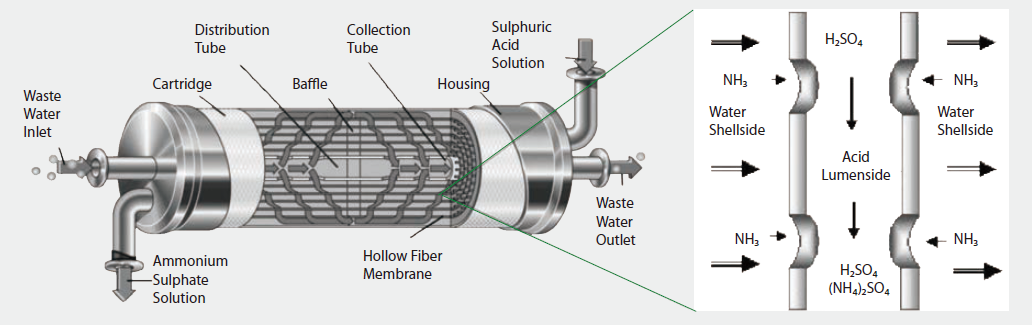
MD去除氨氮的機制與氨分子的亨利常數有關,所以濃縮液在進入MD前,須將pH調到強鹼的條件下形成分子態的氨,如Eq1及 圖五所示,分子態的氨再經由擴散作用通過經非極性處理MD膜,與膜另一側的硫酸進行反應行成硫酸銨,如Eq2。
NH4++OH- ↔ NH3(g)+H2O(l) --------Eq1
2NH3+H2SO4 ↔ (NH4)2SO4 --------Eq2
圖六、氨在MD 內的擴散反應途徑
以MD來去除氨的操作條件,最重要的操作因子是pH,由 表二我們可以發現在入水=1CMH、H2SO4 = 1CMH、pH11.8的操作條件下,以兩段式MD的方式來操作,Ammonia的去除率可達93%。同樣的條件,我們將入水的流量降低到0.5CMH時,兩段式的MD對Ammonia的去除率可達99%。
|
Raw Water Flow Rate (CMH) |
S2SO4 Flow Rate (CMH) |
MD inlet |
1st MD outlet |
2nd MD outlet |
||||||
|---|---|---|---|---|---|---|---|---|---|---|
|
PH |
NH4+ |
Cond |
PH |
NH4+ |
Cond (ms/cm) |
PH |
NH4+ |
Cond (ms/cm) |
||
|
1 |
1 |
11.80 |
2800 |
15.97 |
11.80 |
800 |
16.00 |
11.80 |
200 |
15.95 |
|
0.5 |
1 |
11.80 |
3600 |
15.94 |
11.80 |
180 |
16.09 |
11.80 |
30 |
16.08 |
|
0.5 |
1.5 |
11.80 |
3680 |
15.58 |
11.80 |
160 |
16.00 |
11.80 |
34 |
16.02 |
|
0.4 |
1.6 |
11.80 |
2800 |
15.10 |
11.80 |
130 |
15.90 |
11.80 |
8 |
16.01 |
基本上我們採循環硫酸的操作,藉由吸附來提濃硫酸氨的濃度到25%以上,即可委外處理硫酸銨當工業化產品使用或製造成氨水或其它工業化原料。
結論與展望
因應政府新的排放法規實施在即,在現有含氨氮廢水的處理上,我們可利用前述的處理單元流程來針對此廢水做處理。利用活性碳先將H2O2這類強氧化性物質做去除,以適於後續單元處理;接著經RO 在pH<6.5的環境下,對廢水中氨的去除率可達99%以上;最後再處理RO濃縮水側之高濃度氨廢水,我們使用MD,在廢水和硫酸兩者流速上的比例搭配及MD的設計組合,可達到99%的氨去除率及得到高濃度的硫酸銨產品供後續利用。
針對含氨氮鹼性廢水,我們以各種處理單元設備一步一步以最精簡且有效的流程來做處理、最佳化各單元的處理條件、對流程各產物亦以回收再利用概念降低系統廢水排放。
參考文獻
- 申永順、李崑池、顧洋,1992 ,"以紫外線/過氧化氫程序處理含氯酚類水溶液反應行為之研究"。
- Wiesler W ," Using 'TransMembrane ChemiSorption' (TMCS) for Ammonia removal from Industrial Waste Waters”


留言(0)